이번에는
정압비열과 정적비열에 대한 개념을
설명하겠습니다.
※ 이번 포스팅의 소제목 내부링크
1. 비열의 도출 : 상태도
비열은
물질마다 다른 고유특성값입니다.
하지만, 물질의 상태에 따라
달라질 수 있습니다.
이전에 순물질의 상태도에 대한 설명을 하였습니다.
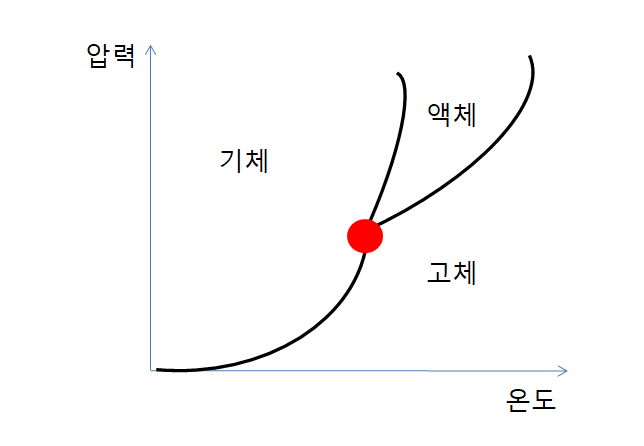
물질마다 상태도가 다릅니다.
비열도 물질의 특성이라 다른데,
압력변화 또는 부피변화를 통하여
1도 올리는데 필요한 열량이 달라집니다.
하지만, 이에 대한 것을 쉽게 계산하기 위해
정압비열과 정적비열을 도출하였습니다.
여기서,
엔탈피, 비열, 열량단위는 단위질량당 에너지로 표시하겠습니다.(kJ/kg)
2. 정압비열 (c_p)
압력이 일정한 상태에서의 비열입니다.
압력이 일정하다는 것은
(외부 열출입량은 항상 들어온다고 가정하고,)
역학적인 에너지의 변화량에 의하여
압력은 변하지 않아도, 부피는 변화합니다.
그래서, 일(W)이 존재합니다.
물질의 열에너지는 내부에너지와 일을 모두 고려해야 하기 때문에,
정압비열은
엔탈피의 함수라고 볼 수 있습니다.
dh = c_p(T) dT
3. 정적비열 (c_v)
부피가 일정한 상태에서의 비열입니다.
부피가 일정하다는 것은
외부에서 보기에 변화가 없습니다.
역학적인 변화가 없기 때문에 일은 없는 것이고,
열은 온도에 의한 직접적인 출입밖에 없어
(외부 열출입량은 항상 들어온다고 가정하고,)
정적비열은 내부에너지의 함수입니다.
du = c_v(T) dT
4. 정압,정적비열 특성
당연히 물질마다 특성이 다르며,
온도구간에 따라도 이 값들이 달라집니다.
(물질 구조와 상태가 달라지면 당연히 열에너지 저장공간도 달라지겠죠.)
이상으로 정압비열, 정적비열에 대한 포스팅을 마치겠습니다.
다음에는
엔트로피에 대한 설명을 하겠습니다.
5. 엔트로피 개념과 이해 (링크)
열역학, 에너지에서 중요한 것이 엔트로피입니다.
자세한 것은 링크를 참조하기 바랍니다.
앞으로도 엔지니어에게 좋은 지식과 정보를 이해하기 쉽게 글을 포스팅하겠습니다. (By. 요르문간드)
'설계지식-열&유체&엔진 > 열역학(기본)' 카테고리의 다른 글
| (엔트로피) 가역, 비가역과정의 이해 (0) | 2023.02.27 |
|---|---|
| 엔트로피 개념과 이해(열역학 제2법칙) (0) | 2023.02.24 |
| 내부에너지와 엔탈피의 개념과 이해 (0) | 2023.02.22 |
| 열역학 0법칙에 대한 개념과 이해(열평형상태) (0) | 2023.02.21 |
| 열량과 비열에 대한 개념 (0) | 2023.02.18 |




댓글